热点推荐
热门图文
例例在望微专辑
可查看更多内容
黎滨茹,马锐丨辽宁省肿瘤医院 胸内二科
III期非小细胞肺癌病情复杂,治疗棘手,围术期管理更是面临诸多挑战。Checkmate816生存数据揭示新辅助免疫获益的同时,“夹心饼”模式的长EFS也给患者带来新的希望,哪种更优?本次病例讨论将聚焦于此,通过具体病例剖析III期肺癌的复杂性,探讨多学科诊疗(MDT)模式的必要性,寻找破局之道。

马锐 教授
学术兼职:中国临床肿瘤学会理事会理事,中国老年学学会老年肿瘤专业委员执行委员,中国老年学学会老年肿瘤专业委员肺癌分委会常务委员,中国医药教育协会肺部肿瘤专委会常务委员,辽宁省生命科学学会常务理事,中国抗癌协会肺癌专业委员会委员,辽宁省抗癌协会理事会理事,辽宁省生命科学学会肺癌专业委员会主任委员,辽宁省抗癌协会肿瘤转移专业委员会主任委员,辽宁省抗癌协会肿瘤标志物专业委员会副主任委员,辽宁省医学会内科学分会委员会常务委员,辽宁省生命科学学会老年肿瘤专业委员会常务委员,沈阳市医学会肺部肿瘤学分会副主委,中国肿瘤生物治疗杂志、中国实用内科、医学与哲学,沈阳医学院学报等多家杂志编委及审稿专家。沈阳市领军人才。
主持省部级、市级课题9项,获辽宁省科技进步三等奖2项、沈阳市科技进步二等奖1项,第一及通讯作者发表论文50余篇。

黎滨茹 教授
中国抗癌协会个案管理专业委员会会员,辽宁省细胞生物学学会肿瘤精准医疗大数据管理专业委员会青年学组理事青年委员 ,CSCO会员,“福维行者”病例演讲比赛京北赛区一等奖
主要研究方向为肺癌的发病机制及分子靶向治疗及免疫治疗。参与省部级课题2项,发表SCI论文4篇,中文论文2篇
病例1
患者刘XX,男,65岁,2021年6月以“右胸痛2个月”为主诉入院,NRS7分,PS1分,吸烟30年,每天20支。外院胸部ct提示:右肺上叶团块影,PET/CT提示:右肺上叶前段可见不规则软组织肿块,范围约68mmx47mm,SUVmax=16.7,病变侵犯胸壁及右侧第4前肋;右肺上叶另见肿块及小结节,葡萄糖代谢增高。纵隔4R淋巴结代谢略增高,右肺上叶前段肺内转移;右肺门淋巴结代谢略增高,SUVmax=3.7,纵隔4R及右肺门淋巴结转移可能性大,未见胸膜增厚及胸腔积液,肝内钙化灶;气管镜取得病理,结合免疫组化为鳞状细胞癌,PD-L1 (22C3) CPS =15。cT3N2M0 IIIB期,经MDT讨论后,为潜在可切除者先行免疫联合化疗,进行转化治疗,替雷利珠单抗+白蛋白紫杉醇/卡铂治疗3周期治疗,评效为缩小的SD。NRS 2分。
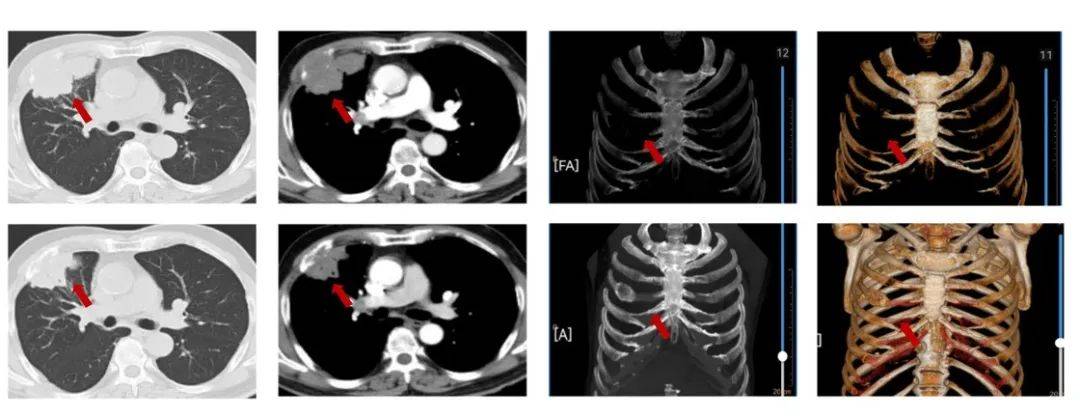
图1:由上至下分别展示基线(A.)及免疫化学治疗后改变(B.)。红色箭头指示病灶位置,由左至右分别为右肺肿物肺窗、右肺肿物纵隔窗、肋骨三维重建。
患者新辅助治疗无严重不良反应 末梢神经炎I级,白细胞减少I级,心肺功能良好,3周期新辅助治疗后无手术禁忌证,患者于2021-09-02我院外科手术切除,术式:胸腔镜辅助下右肺上叶及部分中叶切除,下叶楔形切除,右侧第4肋骨部分切除,肺门纵隔淋巴结清除,胸腔粘连松解术。术后病理:肿物范围约5.2*2.6*2cm,侵透胸膜,侵及肋骨,肋骨长9.5cm,右肺上叶:见癌组织片巢状分布,浸润性生长,局部侵骨组织,见大量坏死。结合免疫组化及病史,鳞状细胞癌伴治疗后改变,侵骨组织。右肺下叶:纤维组织增生多量炎细胞浸润。淋巴结未见转移癌0/32:(D1)2组0/6、(D2)4组0/5、(D3)7组0/3、(D4)8组0/2(D5)10组0/7、(D6)11组0/3、(D7)12组0/2、(D8)13组0/2、(D9)14组0/2。pT3N0M0 IIB期,未达到MPR。术后行8周期替雷利珠单抗辅助治疗。目前患者生活质量良好,DFS已超过4年,仍在定期随访中。
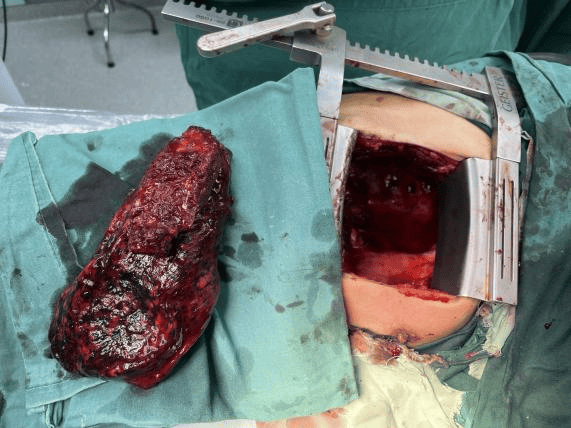
图2:患者手术标本,为肿瘤组织及肋骨成分。
病例2
患者王XX,男,54岁,2023年4月以“咳嗽1个月”入院,PS1分,高血压3年,行替米沙坦40毫克日1次口服血压控制好,否认冠心病, 糖尿病等病史,吸烟史:吸烟30年,每天20支 。肺CT (外院,2023-3):右肺中叶肿物,32mm*37mm,边缘见分叶,纵隔淋巴结肿大,右肺中叶中心型肺癌?邻近上叶前段局部受累不除外。右肺中叶炎症。双肺气肿、肺大泡。肝脏多发小囊肿。支气管镜:右肺中叶见新生物,表面有坏死物附着,堵塞管腔,取病理。病理:鳞癌。PD-L1(DAKO 22C3)(+,CPS=20)。cT2bN2M0,ⅢA期。经MDT讨论后,患者为可切除手术患者,建议新辅助治疗。给予患者3周期特瑞普利单抗+紫杉醇/卡铂治疗,3周期评效PR。
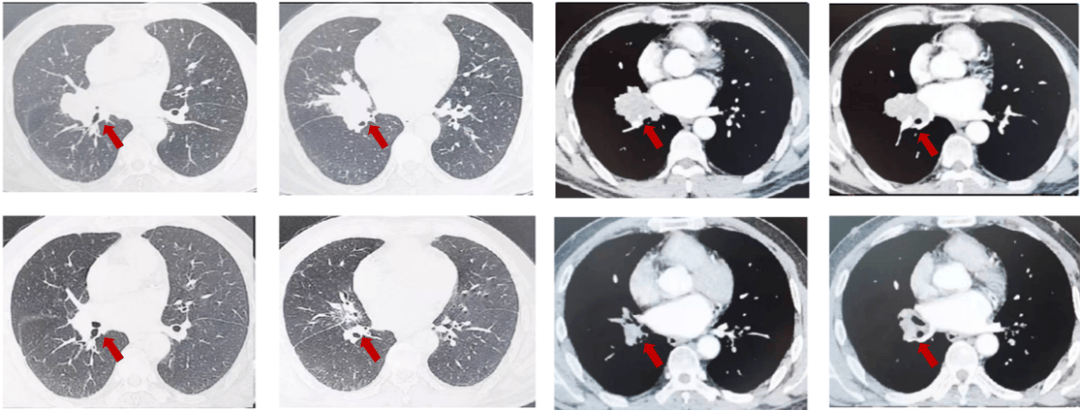
图3:由上至下分别展示基线(A.)及免疫化学治疗后改变(B.)。红色箭头指示病灶位置,由左至右分别为右肺肿物肺窗、右肺肿物纵隔窗。
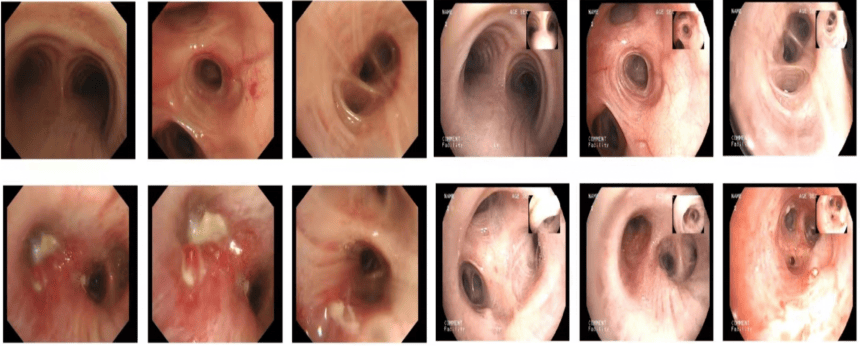
图4:由左至右分别展示基线(A1-3)及免疫化学治疗后改变(B4-6)。支气管开口肿瘤明显退缩,结合影像判断达PR。
患者2023年7月,于我院行单孔胸腔镜下右肺中下叶切除,肺门纵隔淋巴结清扫、胸膜粘连松解术。术后病理:(右肺中下叶)治疗后标本,未见癌细胞,符合治疗后改变,请密切结合原病理报告。(淋巴结)未见转移癌0/17,2组 0/5,4 组0/2 ,7组 0/2,8组0/1 , 9组 0/2 ,10组 0/2 ,11 组0/2,12 组0/1 。pT0N0M0,达PCR,术后行1周期特瑞普利单抗+紫杉醇/卡铂治疗,13周期特瑞普利单抗维持治疗,DFS23个月,目前随访中。
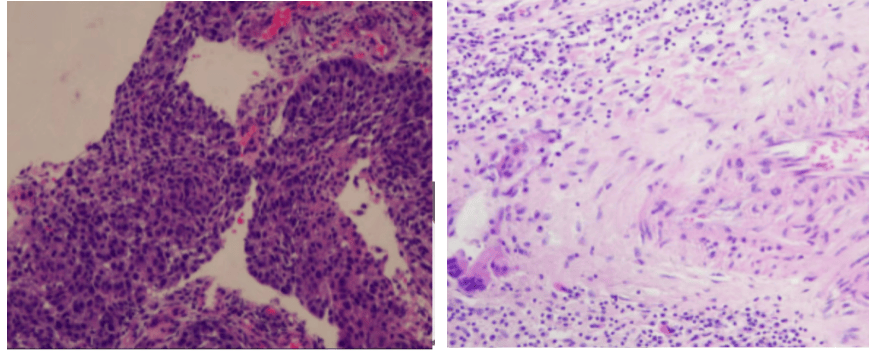
图5:由左至右分别展示病理基线(A)及免疫化学治疗后术后病理图片(B)。
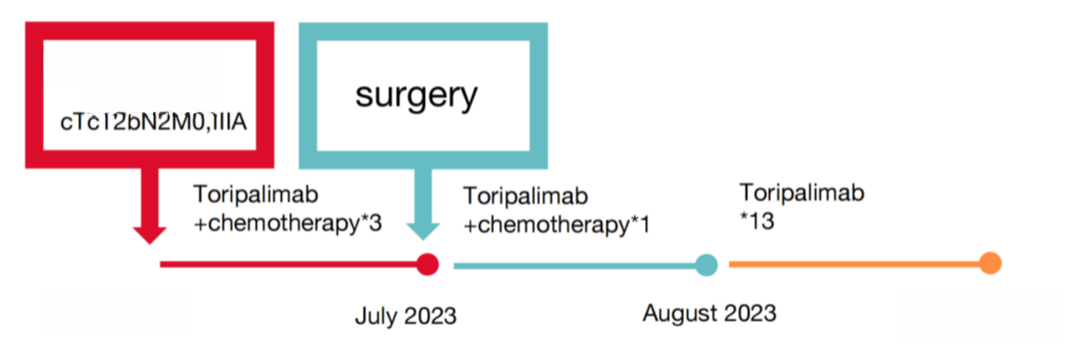
图6:患者诊疗经过流程图
病例讨论
III期非小细胞肺癌的治疗选择多样且复杂,尤其近年来免疫治疗走进新辅助后的高PCR及MPR率让许多初始不可切或难切的肿瘤变为可切除,从而改变预后。III期肺癌更需要MDT诊疗,同时我们还在疑问新辅助和夹心饼(即新辅助治疗+手术+辅助治疗)模式哪种更好?还悬而未决!
RATIONALE-315和NEOTORCH同为“夹心饼”模式的代表研究。RATIONALE-3151主要终点EFS:替雷利珠单抗组患者无事件生存期明显改善(HR=0.56,95%CI:0.40-0.79,P=0.0003)。OS:替雷利珠单抗组呈明显较好趋势,(HR=0.62,95%CI:0.39-0.98,P=0.0193)。NEOTORCH2,3是全球首个抗PD-1单抗在NSCLC围手术期达到EFS阳性结果的III期研究。主要终点:特瑞普利单抗组中位EFS未达到,对照组为15.1个月(HR=0.40,P<0.001),夹心饼模式在国内已有多款PD-1制剂获批适应症且进入医保,在中国临床实践中采用此模式的治疗也许会更多。
KEYNOTE-671也是个夹心饼模式4,在可切除的II-IIIB期非小细胞肺癌(NSCLC)患者中的疗效和安全性的III期临床试验。KEYNOTE-671以EFS, OS 为双研究终点设计试验。EFS结果:帕博利珠单抗联合化疗组的24个月EFS率为62.4%,而安慰剂联合化疗组为40.6%(HR=0.58,95% CI:0.46-0.72,P<0.00001)在2024年的更新数据中5,帕博利珠单抗组的中位EFS延长至57.1个月,安慰剂组为18.4个月。OS结果:帕博利珠单抗组的中位OS未达到,安慰剂组为52.4个月(HR=0.72,95% CI:0.56-0.93,P=0.00517)。
作为单纯新辅助免疫治疗的代表研究,CheckMate-816是第一个评估新辅助免疫治疗联合化疗与单独化疗在可切除NSCLC中的安全性和有效性的III期临床试验6。2025年ASCO会议数据更新7,在68.4个月的中位随访中,纳武单抗联合化疗组(n = 179)与单独化疗组(n = 179)相比,中位总生存期未达到(NR),死亡风险降低28% 3(HR, 0.72;95% CI:0.523-0.998;P= 0.0479)。纳武单抗联合化疗组的60个月OS率为65%,单独化疗组为55%,提高10%。纳武单抗联合化疗组的中位EFS为59.6个月,单独化疗组为21.1个月(HR, 0.68;95% CI:0.51-0.91)。纳武单抗联合化疗组pCR患者5年总生存率为95.3% (95% CI:82.7-98.8),pCR患者中仅有3例死亡于非肺癌相关事件。在接受纳武利尤单抗联合化疗的患者中,ctDNA清除率较高56%,且ctDNA清除的患者中46%获得了pCR。相比之下,ctDNA未清除的患者中无pCR。
结论
CheckMate 816中报告的生存获益与围手术期“夹心饼”式免疫治疗EFS改善方面具有相似的趋势;然而,跨试验的直接比较应谨慎解释。那么,围术期选择何种模式?期待头对头的临床研究给出答案。
参考文献:
(上下)
1.Yue D, Wang W, Liu H, et al. Perioperative tislelizumab plus neoadjuvant chemotherapy for patients with resectable non-small-cell lung cancer (RATIONALE-315): an interim analysis of a randomised clinical trial. Lancet Respir Med. 2025 Feb;13(2):119-129.
2.Lu S, Zhang W, Wu L, et al. Perioperative Toripalimab Plus Chemotherapy for Patients With Resectable Non-Small Cell Lung Cancer: The Neotorch Randomized Clinical Trial [published correction appears in JAMA. 2025 Feb 10. doi: 10.1001/jama.2025.0962.]. JAMA. 2024;331(3):201-211. doi:10.1001/jama.2023.24735.
3.Shun L. Perioperative Toripalimab + Platinum-Doublet Chemotherapy vs Chemotherapy in Resectable Stage ll/lll Non-small Cell Lung Cancer:Interim Event-Free Survival Analysis of the Phase Ill Neotorch Study [M]. ASCO Monthly Plenary Series (April). 2023.
4.Wakelee H, Liberman M, Kato T, et al. KEYNOTE-671: Randomized, double-blind, phase 3 study of pembrolizumab or placebo plus platinum-based chemotherapy followed by resection and pembrolizumab or placebo for early stage NSCLC. 2023 ASCO Annual Meeting. Abstract LBA100. Presented June 3, 2023.
5.Spicer JD, Garassino MC, Wakelee H, et al. Neoadjuvant pembrolizumab plus chemotherapy followed by adjuvant pembrolizumab compared with neoadjuvant chemotherapy alone in patients with early-stage non-small-cell lung cancer (KEYNOTE-671): a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet. 2024;404(10459):1240-1252.
6.CheckMate 816 Investigators. (2022). Neoadjuvant Nivolumab plus Chemotherapy in Resectable Lung Cancer. New England Journal of Medicine, 386(21), 1973-1985.
7.2025 ASCO LBA8000.
